Sia u cumposti chimichi cum'è l'elementi chimichi sò custituiti da molecule, è queste à u so turnu sò cumposte da atomi. L'atomi fermanu uniti grazia à a furmazione di i cosiddetti ligami chimichi.
U i ligami chimichi ùn sò micca tutti listessi: basicamente dipendenu da e caratteristiche elettroniche di l'atomi implicati. Ci hè dui tippi più cumuni di ligami: ligami ionichi è u ligami covalenti.
Tipicamente, i ligami covalenti sò quelli chì tene inseme atomi non metallichi. Accade chì l'atomi di questi elementi anu parechji elettroni in u so cunchju uperifericu è anu una tendenza à mantene o guadagnà elettroni, invece di rinuncià à elli.
Hè per quessa u modu in quale queste sostanze o cumposti chimichiicos ghjunghje stabilità hè da spartendu una coppia di elettroni, umicca da ogni atomu. In questu modu a coppia cumuna di elettroni hè cumuna à i dui atomi è à u listessu tempu li tene inseme. In u gasi nobili, per esempiu, accade questu. Ancu in elementi alogeni.
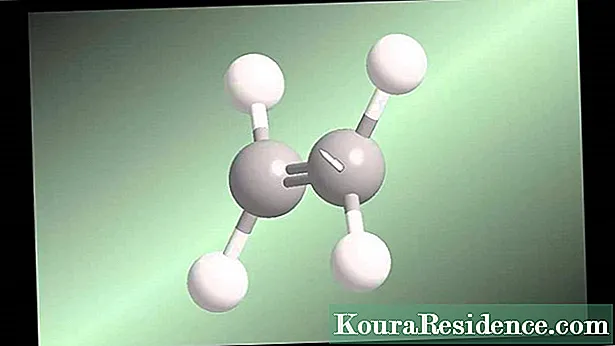
Quandu u legame covalente si faci trà elementi di elettronegatività simile, cume trà l'idrogenu è u carbonu, si genera un legame covalente apulare. Questu accade, per esempiu, in idrocarburi.
In listessu modu, si formanu sempre molecule omonucleari (cumposte da u listessu atomu) ligami apolari. Ma se u ligame si faci trà elementi di diversa electronegatività, una densità di elettroni più alta hè prodotta in un atomu chè in un altru, per via di questu hè furmatu un polu.
Una terza pussibilità hè chì dui atomi spartinu una coppia di elettroni, ma chì sti elettroni spartuti sò cuntribuiti da solu un atomu di elli. In questu casu parlemu di ligame covalente dativu o coordinatu.
Per un ligame dativu avete bisognu di un elementu cù una coppia di elettroni liberi (cum'è u nitrogenu) è un altru chì hè carente di elettroni (cum'è l'idrogenu). Hè ancu necessariu chì quellu cù a coppia elettronica sia abbastanza elettronegativu per ùn perde l'elettroni da sparte. Sta situazione si verifica, per esempiu, in ammoniaca (NH4+).
U sustanzi chì cuntenenu cumposti covalenti ponu accade in ogni statu di materia (solidu, liquidu o gassosu), è in generale sò cunduttori poveri di calore è elettricità.
Spessu mostranu punti di fusione è ebullizione relativamente bassi è sò generalmente solubili in solventi polari, cum'è u benzene o u tetracloruru di carbonu, ma anu poca solubilità in acqua. Sò estremamente stabili.
Numerosi esempi di cumposti o sostanze chì cuntenenu ligami covalenti ponu esse dati:
- Fluoru
- Bromu
- Iodiu
- Cloru
- Ossigenu
- Acqua
- Diossidu di carbonu
- Ammoniaca
- Metanu
- Propanu
- Silice
- Diamante
- Grafit
- Quartz
- Glucosiu
- Paraffina
- Diesel
- Azotu
- Eliu
- Freon